بسم الله الرحمن الرحيم
السلام عليكم ورحمة الله تعالى وبركاته
حل أسئلة 2-2 درس تغيرات المادة – المادة – الخواص والتغيرات.
نبدأ على بركة الله ...
ماذا قرأت؟
ماذا قرأت؟ عرف التفاعل الكيميائي.
الحل:
التغير الكيميائي هو تغير مادة أو أكثر إلى مواد جديدة.
مسائل تدريبة
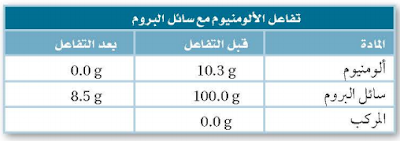
5. استعمل البيانات الموجودة في الجدول للإجابة عن الأسئلة التالية:
كم جراماً من البروم تفاعل، وكم جراماً من المركب نتج؟
الحل:
عدد جرامات البروم المتفاعلة =
عدد جرامات البروم قبل التفاعل – عدد جرامات البروم بعد التفاعل
= 100 – 8.5
= 91.5 جرام
6. حصل طالب في تجربة لتحليل الماء على 10.0 g هيدروجين و79.4 g أكسجين. ما مقدار الماء المستعمل في هذه العملية؟
الحل:
نستخدم قانون حفظ الكتلة الذي ينص على أن كتلة المتفاعل = كتلة الناتج
كتلة الماء المتفاعل = كتلة الماء المتحلل
كتلة الماء المتحلل = كمية الأكسجين + كمية الهيدروجين
= 10 + 79.4
= 89.4 جم ماء.
7. أضاف طالب 15.6 g صوديوم إلى كمية وافرة من غاز الكلور، وبعد انتهاء التفاعل حصل على 39.7 g من كلوريد الصوديوم. ما كتلة كل من الكلور والصوديوم المتفاعلين؟
الحل:
نستخدم قانون حفظ الكتلة الذي ينص على أن كتلة المتفاعل = كتلة الناتج
كتلة الصوديوم والكلور المتفاعل = كتلة كلوريد الصوديوم الناتج.
المعطيات:
كتلة كلوريد الصوديوم= 39.7 جم
كتلة الصوديوم= 15.6 جم
كتلة الكلور = ؟
تطبيق القانون:
كتلة الكلور + كتلة الصوديوم = كتلة كلوريد الصوديوم
؟ +15.6 = 39.7
ولإيجاد كتلة الكلور نقوم بطرح كتلة الصوديوم من كتلة كلوريد الصوديوم.
كتلة الكلور = 39.7 – 15.6
= 24.1 جم.
8. تفاعلت عينة مقدارها 10.0 g من الماغنسيوم مع الأكسجين لتكوين 16.6 g من أكسيد الماغنسيوم. كم جراماً من الأكسجين تفاعل؟
الحل:
نستخدم قانون حفظ الكتلة الذي ينص على أن كتلة المتفاعل = كتلة الناتج
كتلة الماغنسيوم والأكسجين المتفاعل =كتلة أكسيد الماغنسيوم
المعطيات:
كتلة أكسيد الماغنسيوم = 16.6 جم
كتلة الماغنسيوم = 10 جم
كتلة الأكسجين =؟
تطبيق القانون:
كتلة الأكسجين + كتلة الماغنسيوم = كتلة أكسيد الماغنسيوم
؟ + 10 = 16.6
ولإيجاد كتلة الأكسجين نقوم بطرح كتلة الماغنسيوم من كتلة أكسيد الماغنسيوم.
كتلة الأكسجين = 16.6 – 10
= 6.6 جم.
9. تحفيز تفاعل 106.5 g من حمض الهيدروكلوريك HCl (g) مع كمية مجهولة من الأمونيا NH3(g) لإنتاج 157.5 g من كلوريد الأمونيوم NH4Cl(s). ما كتلة الأمونيا NH3(g) المتفاعلة؟ وهل طبق قانون حفظ الكتلة في هذا التفاعل؟ فسر إجابتك.
الحل:
نستخدم قانون حفظ الكتلة الذي ينص على أن كتلة المتفاعل = كتلة الناتج
كتلة الأمونيا وحمض الهيدروكلوريك المتفاعلة = كتلة كلوريد الأمونيا الناتج
المعطيات:
كتلة كلوريد الأمونيا = 157.5 جم
كتلة حمض الهيدروكلوريك = 106.5 جم
كتلة الأمونيا =؟
تطبيق القانون:
كتلة الأمونيا + كتلة حمض الهيدروكلوريك = كتلة كلوريد الأمونيا
؟ + 106.5 = 157.5
ولإيجاد كتلة الأمونيا نقوم بطرح كتلة حمض الهيدروكلوريك من كتلة كلوريد الأمونيا.
كتلة الأمونيا = 157.5 – 106.5
= 51 جم.
التقويم 2-2
10. الفكرة الرئيسة صنف الأمثلة إلى تغيرات فيزيائية أو كيميائية.
a. سحق علبة ألومنيوم.
الحل:
تغير فيزيائي.
b. تدوير علب الألومنيوم المستعملة لإنتاج علب جديدة.
الحل:
تغير فيزيائي.
c. اتحاد الألومنيوم مع الأكسجين لإنتاج أكسيد الألومنيوم.
الحل:
تغير كيميائي.
11. صف نتائج التغير الفيزيائي، وأعط ثلاثة أمثلة عليه.
الحل:
التغير الفيزيائي هو تغير في مظهر المادة، ولكن يظل تركيبها الكيميائي ثابت لا يتغير مثل تشكيل صفيحة نحاس لكرة، تحول الجليد لماء، تكسير لوح زجاجي.
12. صف نتائج التغير الكيميائي، واذكر أربعة أدلة على حدوثه.
الحل:
التغير الكيميائي هو تحول المادة إلى مادة جديدة مختلفة التركيب والخواص وذلك بحدوث تفاعل كيميائي لها. وهناك أدلة على حدوث التغيير الكيميائي منها تغير اللون، تغير الطعم والرائحة وتغيير الخواص الفيزيائية مثل الكثافة والانجذاب للمغناطيس.
13. احسب. حل المسائل الآتية:
a. إذا تفاعل 22.99 g من الصوديوم تماماً مع 35.45 g من الكلور فما كتلة كلوريد الصوديوم الناتج؟
الحل:
نستخدم قانون حفظ الكتلة الذي ينص على أن كتلة المتفاعل = كتلة الناتج
كتلة الصوديوم والكلور المتفاعلة = كتلة كلوريد الصوديوم الناتج
المعطيات:
كتلة الصوديوم = 22.99 جم
كتلة الكلور = 35.45 جم
كتلة كلوريد الصوديوم =؟
تطبيق القانون:
كتلة الصوديوم + كتلة الكلور = كتلة كلوريد الصوديوم
22.99 + 35.45= 58.44 جم
b. إذا تفاعل 12.2 g من مادة X مع عينة من Y ونتج 78.9 g من XY فما كتلة Y المتفاعلة؟
الحل:
نستخدم قانون حفظ الكتلة الذي ينص على أن كتلة المتفاعل = كتلة الناتج
المعطيات:
كتلة المادة X = 12.2 جم
كتلة المادة Y =؟
كتلة المادة XY = 78.9 جم
تطبيق القانون:
كتلة المادة X + كتلة المادة Y = كتلة المادة XY
12.2 +؟ = 78.9 جم
ولإيجاد كتلة المادة Y نقوم بطرح كتلة حمض المادة X من كتلة المادة XY.
المادة Y = 78.9 – 12.2
= 66.7 جم
14. قوم إذا قال لك صديق:" إذا كان تركيب المادة لا يتغير خلال التغير الفيزيائي فإن مظهرها لا يتغير ". فهل هو على صواب؟ فسر إجابتك.
الحل:
لا، ليس صواب لأن التغير الفيزيائي يصاحبه تغير في المظهر، ولكن لا يحدث أي تغيير في تركيب المادة.
تم بحمد الله
نستقبل أسئلتكم واستفساراتكم واقتراحاتكم في خانة التعليقات
"نرد على جميع التعليقات"
بالتوفيق للجميع...^-^










ليست هناك تعليقات:
إرسال تعليق