بسم الله الرحمن الرحيم
السلام عليكم ورحمة الله وبركاته
ملخص 1-4 التفاعلات والمعادلات - التفاعلات الكيميائية
نبدأ على بركة الله ...
التفاعل الكيميائي: هي العملية التي يعاد فيها ترتيب الذرات في مادة أو أكثر لتكوين مواد مختلفة.
مؤشرات حدوث التفاعل الكيميائي
· تغير درجة الحرارة، إطلاق طاقة على شكل ضوء وحرارة أو امتصاص حرارة.
· تغير اللون، تغير الرائحة، تصاعد الغاز، تكون مادة صلبة.
مثال على مؤشر حدوث تفاعل:
تحول لون الموز من الأخضر إلى الأصفر.
التوزيع الإلكتروني:
كل مستوى (n) من مستويات الطاقة الرئيسة يسع عددًا محدداً من الإلكترونات.
أقصى عدد من الإلكترونات يستوعبه مستوى الطاقة الرئيس يمكن حسابه بالمعادلة: e=2n2.
الإلكترونات تتوزع في مستويات طاقة ثانوية مختلفة الشكل والطاقة يشار إليها بالأحرف (f,d,p,s).
تتوزع الطاقة ضمن مستويات الطاقة الرئيسية في مستويات طاقة فرعية داخل مستويات الطاقة الثانوية بدءا من الأقل طاقة.
من استثناءات التوزيع الإلكتروني
(خطأ) التوزيع المتوقع لذرة النحاس/ Cu29: 1s2 2s2 2p6 3s2 3p6 4s2 3d9
(صح) التوزيع الصحيح لذرة النحاس/ Cu29: 1s2 2s2 2p6 3s2 3p6 4s1 3d10
(خطأ) التوزيع المتوقع لذرة الكروم/ Cr24: 1s2 2s2 2p6 3s2 3p6 4s2 3d4
(صح) التوزيع الصحيح لذرة الكروم/ Cr24: 1s2 2s2 2p6 3s2 3p6 4s1 3d5
الرموز والصيغ
رموز العناصر وعدد أكسدتها
الرمز: حرف أو حرفان مشتقان من اسم العنصر للدلالة عليه.
رموز بعض العناصر وعدد أكسدتها
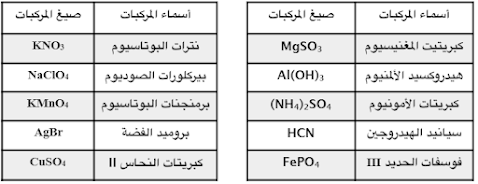
صيغ الأيونات عديدة الذرات وأعداد أكسدتها
الصيغة: مجمعة من الرموز لدلالة على المركب أو الأيون عديد الذرات (الشقوق)
صيغ الأيونات
عديدة الذرات الشقوق وعدد أكسدتها


التوزيع الإلكتروني
ترتيب المستويات الإلكترونية ss ps ps dps dps fdps fdp
2s2 2p6/ 3s2 3p6/1s2
4s2 3d10 4p6/ 5s² 4d10 5p6/
6s2 4f14 5d10 6p6/ 7s² 5f14 6d10 7p6
المستويات الرئيسة: سبعة مستويات (1,2,3,4,5,6,7(
المستويات الثانوية: أربعة مستويات ( s,p,d,f)
المستويات الفرعية:)عدد الغرف (7=1 ,p=3, d= 5 , f= s
عدد الإلكترونات في المستويات الفرعية s = 2 ,p=6 ,d=10,f= 14
كتابة الصيغ الكيميائية لكتابة الصيغ الكيميائية لابد أن تعرف أولا عدد تأكسد تكافؤ العنصر.
عدد التأكسد: هو عدد الإلكترونات التي تفقدها أو تكتسبها أو تشارك بها ذرة العنصر في أثناء التفاعل الكيميائي.
تسمية المركبات الأيونية هناك خطوات وقواعد للتسمية.
خطوات تسمية المركبات الأيونية:
1- يسمى الأيون السالب أولا متبوعا باسم الأيون الموجب.
2- في حالة الأيون السالب الأحادي الذرة يشتق الاسم من اسم العنصر مضافا إليه المقطع (يد).
3 - عند وجود أكثر من عدد تأكسد لأيون الموجب يجب أن تشير إلى عدد التأكسد بالأرقام اللاتينية بعد اسم موجب، أحادي I، ثنائي II، ثلاثي III، رباعي IV، خماسي V.
4- عندما يحتوي المركب على أيون عديد الذرات نقوم بتسميته أولا ثم نسمي الأيون الموجب.
أمثلة توضح كتابة صيغ المركبات الأيونية:
وأكسيد الألمونيوم Al2O3 وكلوريد الكوبلت CoCl2 II وهيدروكسيد الصوديوم NaOH.
مثال على ذلك: كلوريد الصوديوم NaCl NaBr وبروميد الصوديوم،
وكرومات الفضة Ag2CrO4 ونترات النحاسII Cu (NO3)2 وأكسيد الحديدII FeO وأكسيد الحديدIII FezO3.
المتفاعلات: وهي المواد التي توجد عند بداية التفاعل.
النواتج: وهي المواد المتكونة خلال التفاعل.
تستخدم الرموز في المعادلات لتوضيح الحالة الفيزيائية لكل مادة متفاعلة أو ناتجة.
(s) يشير إلى الحالة الصلبة، (I) يشير إلى الحالة السائلة.
(g) يشير إلى الحالة الغازية، (aq) يشير إلى المحلول المائي.
المعادلات الكيميائية اللفظية: يمكنك استعمال المعادلات ال لفظية للتعبير عن كل من المواد المتفاعلة والناتجة في التفاعلات الكيميائية.
بروميد الألومنيوم → البروم + الألومنيوم
المعادلات الكيميائية الرمزية: تستخدم رموز العناصر وصيغ المركبات في المعادلات الكيميائية الرمزية للتعبير عن المتفاعلات والنواتج.
Al(s) + Br2(I) → AlBr3
المعادلات الكيميائية الرمزية الموزونة: تشبه المعادلات الرمزية المعادلات ال لفظية في أنها تفتقر إلى معلومات مهمة عن التفاعلات.
32AIB→ 2Al(s) + 3Br2(I)
قانون حفظ الكتلة:
"ينص على أنه خلال التغير الكيميائي لا تفنى المادة ولا تستحدث".
لتمثيل التفاعل الكيميائي بمعادلة صحيحة نستخدم (المعادلة الكيميائية الرمزية الموزونة).
المعادلات الكيميائية الرمزية الموزونة: تعبير يستخدم الصيغ الكيميائية لتوضيح أنواع المواد المتضمنة في التفاعل الكيميائي وكمياتها النسبية.
وزن المعادلات الكيميائية
· لكي تزن المعادلات الكيميائية يجب أن تجد المعاملات الصحيحة للصيغ الكيميائية في المعادلة الرمزية.
المعامل: في المعادلة الكيميائية هو العدد الذي يكتب قبل المادة المتفاعلة أو الناتجة.
· تصف المعاملات في المعادلة الموزونة أبسط نسبة عددية صحيحة لكميات كل من المتفاعلات والنواتج.
تحقيق قانون حفظ الكتلة:
قانون حفظ الكتلة من أهم المفاهيم الأساسية في الكيمياء ويتم تطبيقه في المعادلة الكيميائية بوزنها.
قانون حفظ الكتلة: ينص على أن المادة لا تفني ولا تستحدث إلا بقدرة الله تعالى.
تم بحمد الله
نستقبل أسئلتكم واستفساراتكم واقتراحاتكم في خانة التعليقات
"نرد على جميع التعليقات"
بالتوفيق للجميع...^-^













ليست هناك تعليقات:
إرسال تعليق